Đừng bỏ lỡ những tính năng hấp dẫn của Baitap365.com
Đặc điểm cấu tạo và liên kết kim loại. Tính chất kim loại.
14.1
Ở trạng thái cơ bản, cấu hình electron của nguyên tử Mg (Z = 12) là
A. 1s22s22p63s1. B. 1s22s22p63s2.
C. 1s22s32p63s2. D. 1s22s22p73s1.
14.2
Ở trạng thái cơ bản, cấu hình electron lớp ngoài cùng của nguyên tử X là 3s1. Số hiệu nguyên tử của nguyên tố X là
A. 11. B. 12. C. 13. D. 14.
14.3
Kim loại có những tính chất vât lí chung nào sau đây?
A. Tính dẻo, tính dẫn điện, nhiệt độ nóng chảy cao.
B. Tính dẻo, tính dẫn điện, có khối lượng riêng lớn và có ánh kim.
C. Tính dẻo, tính dẫn điện, tính dẫn nhiệt và có ánh kim.
D. Tính dẻo, có ánh kim, rất cứng.
14.4
Các tính chất vật lí chung của kim loại gây nên chủ yếu bởi
A. các electron tự do trong mạng tinh thể.
B. các ion kim loại.
C. các electron hoá trị.
D. các kim loại đều là chất rắn
14.5
Kim loại X được sử dụng trong nhiệt kế, áp kế và một số thiết bị khác. Ở điều kiện thường, X là chất lỏng. Kim loại X là
A. W. B. Cr. C. Hg. D. Pb.
14.6
Kim loại nào sau đây tan hoàn toàn trong nước?
A. Cu. B. Ag. C. K. D. Au.
14.7
Dãy gồm các kim loại đều phản ứng với nước ở nhiệt độ thường tạo thành dung dịch có môi trường kiềm là
A. Na, Fe, K. B. Na, Cr, K.
C. Na, Ba, K. D. Mg, Na, Ca.
14.8
Trong các kim loại Na, Ca, K, Al, Fe, Cu và Zn, số kim loại tan tốt trong dung dịch KOH là
A. 3. B. 4. C. 5. D. 6.
14.9
Thí nghiệm nào sau đây không sinh ra đơn chất?
A. Cho CaCO3 vào lượng dư dung dịch HCl.
B. Cho kim loại Cu vào dung dịch AgNO3.
C. Cho kim loại Zn vào dung dịch CuSO4.
D. Cho kim loại Mg vào dung dịch HCl.
14.10
Cho dãy các kim loại: Al, Cu, Fe, Ag. Số kim loại trong dãy phản ứng được với dung dịch H2SO4 loãng là
A. 1. B. 2. C. 3. D. 4.
14.11
Cho dãy các kim loại: Fe, Cu, Mg, Ag, Al, Na, Ba. Số kim loại trong dãy phản ứng được với dung dịch HCl là
A. 3. B. 4. C. 5. D. 6.
14.12
Kim loại nào sau đây khi tác dụng với HCl và tác dụng với Cl2 (được nung nóng) tạo thành cùng một sản phẩm muối chloride?
A. Fe. B. Ag. C. Zn. D. Cu.
14.13
Phát biểu nào sau đây là đúng?
A. Ở điều kiện thường, các kim loại đều có khối lượng riêng lớn hơn khối lượng riêng của nước.
B. Tính chất hoá học đặc trưng của kim loại là tính khử.
C. Các kim loại đều chỉ có một oxi hoá duy nhất trong các hợp chất.
D. Ở điều kiện thường, tất cả các kim loại đều ở trạng thái rắn.
14.14
Cho kim loại Fe lần lượt phản ứng với các dung dịch: FeCl3, Cu(NO3)2, AgNO3, MgCl2. Số trường hợp xảy ra phản ứng hoá học là
A. 1. B. 2. C. 3. D. 4.
14.15
X là kim loại phản ứng được với dung dịch H2SO4 loãng, Y là kim loại tác dụng được với dung dịch Fe(NO3)3. Hai kim loại X, Y có thể là
A. Ag, Mg. B. Cu, Fe. C. Fe, Cu. D. Mg, Ag.
14.16
Cho một lá sắt nhỏ vào dung dịch chứa một trong những muối sau: CuSO4, AlCl3, Pb(NO3)2, ZnCl2, KNO3, AgNO3. Viết phương trình hoá học của các phản ứng xảy ra (nếu có). Cho biết vai trò của các chất tham gia phản ứng.
14.17
Hãy giới thiệu phương pháp để làm sạch kim loại sắt có lẫn tạp chất nhôm. Giải thích phương pháp được lựa chọn, viết phương trình hoá học của các phản ứng xảy ra (nếu có).
14.18
Cho Cu tác dụng với dung dịch Fe2(SO4)3 thu được dung dịch hỗn hợp gồm hai chất tan là FeSO4 và CuSO4. Cho vào dung dịch thu được một ít bột sắt thì thấy bột sắt bị hoà tan. Viết phương trình hoá học của các phản ứng xảy ra.
14.19
Sodium và potassium là hai kim loại kiềm có tính khử mạnh. Hãy đề xuất cách bảo quản hai kim loại này. Giải thích
14.20
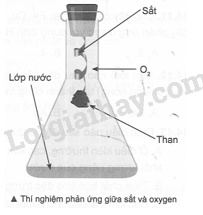
Khi thực hiện thí nghiệm về phản ứng giữa sắt và oxygen, người ta thường cho một ít nước vào trong bình tam giác chứa khí oxygen và cột mẩu than lên thanh dây sắt (như hình bên). Hãy cho biết vai trò của lớp nước dưới đáy bình và mẩu than.
Mẹo tìm đáp án nhanh
Search Google: "từ khóa + baitap365" Ví dụ: "Bài 5 trang 13 SGK Vật lí 12 baitap365