Đừng bỏ lỡ những tính năng hấp dẫn của Baitap365.com
Đề thi giữa kì 1 KHTN 8 - Kết nối tri thức
Đề thi giữa kì 1 KHTN 8 Kết nối tri thức - Đề số 8
Đề thi giữa kì 1 KHTN 8 Kết nối tri thức - Đề số 9 Đề thi giữa kì 1 KHTN 8 Kết nối tri thức - Đề số 10 Đề thi giữa kì 1 KHTN 8 Kết nối tri thức - Đề số 7 Đề thi giữa kì 1 KHTN 8 Kết nối tri thức - Đề số 6 Đề thi giữa kì 1 KHTN 8 Kết nối tri thức - Đề số 5 Đề thi giữa kì 1 KHTN 8 Kết nối tri thức - Đề số 4 Đề thi giữa kì 1 KHTN 8 Kết nối tri thức - Đề số 3 Đề thi giữa kì 1 KHTN 8 Kết nối tri thức - Đề số 2 Đề thi giữa kì 1 KHTN 8 Kết nối tri thức - Đề số 1Đề thi giữa kì 1 KHTN 8 Kết nối tri thức - Đề số 8
Dụng cụ thí nghiệm nào dùng để lấy dung dịch hóa chất lỏng?
Dụng cụ thí nghiệm nào dùng để lấy dung dịch hóa chất lỏng?
Kẹp gỗ.
Bình tam giác.
Ống nghiệm.
Ống hút nhỏ giọt.
Đáp án : D
Dựa vào dụng cụ thí nghiệm.
Để lấy hóa chất lỏng người ta dùng ống hút nhỏ giọt để hút chất lỏng.
Đáp án D
Việc làm nào sau đây không đảm bảo quy tắc an toàn trong phòng thí nghiệm?
Không sử dụng hoá chất đựng trong đồ chứa không có nhãn hoặc nhãn mờ.
Đọc cẩn thận nhãn hoá chất trước khi sử dụng.
Có thể dùng tay trực tiếp lấy hoá chất.
Không được đặt lại thìa, panh vào lọ đựng hoá chất sau khi đã sử dụng.
Đáp án : C
Dựa vào quy tắc an toàn phòng thí nghiệm.
Không được dùng tay trực tiếp lấy hóa chất vì có thể gây bỏng hoặc gây hại cho da.
Đáp án C
Biến đổi hóa học là
hiện tượng chất biến đổi tạo ra chất khác.
hiện tượng chất biến đổi trạng thái
hiện tượng chất biến đổi hình dạng.
hiện tượng chất biến đổi về kích thước
Đáp án : A
Dựa vào khái niệm về biến đổi hóa học.
Biến đổi hóa học là hiện tượng chất biến đổi tạo ra chất khác.
Đáp án A
Thả một đinh sắt vào dung dịch hydrochloric acid ta thấy đinh sắt tan dần và xuất hiện bọt khí, hiện tượng trên là sự biến đổi
vật lí.
hóa học.
vật lí và hoá học.
không phải sự biến đổi nào.
Đáp án : B
Dựa vào sự biến đổi vật lí và biến đổi hóa học.
Khi thả đinh sắt vào dung dịch hydrochloric acid ta thấy đinh sắt tan dần, xuất hiện bọt khí đây là dấu hiệu thể hiện sự biến đổi hóa học.
Đáp án B
Cho khoảng một thìa cafe bột NaHCO3 vào bình tam giác, sau đó thêm vào bình 10 ml dung dịch CH3COOH. Chạm tay vào thành bình ta thấy bình lạnh đi, đây là phản ứng:
thu nhiệt.
tỏa nhiệt.
cả hai phản ứng trên.
không phải phản ứng hóa học.
Đáp án : A
Dựa vào năng lượng phản ứng.
Khi chạm tay vào thành bình ta thấy bình lạnh đi là do phản ứng đã lấy năng lượng từ môi trường đây là phản ứng thu nhiệt.
Đáp án A
Đốt cháy xăng, dầu trong các động cơ là
phản ứng thu nhiệt.
phản ứng tỏa nhiệt.
Phản ứng phân hủy.
phản ứng thế.
Đáp án : B
Dựa vào năng lượng phản ứng.
Khi đốt cháy xăng, dầu trong các động cơ là phản ứng tỏa nhiệt để cung cấp năng lượng để chạy động cơ.
Đáp án B
Thiết bị nào là đồng hồ đo công suất điện ở mạch điện?
Oát kế.
Vôn kế.
Ampe kế.
Áp kế
Đáp án : A
Dựa vào các dụng cụ đo.
Để đo công suất điện ở mạch điện người ta sử dụng oát kế.
Đáp án A
Bánh mì nướng bị cháy là quá trình của:
sự biến đổi hóa học.
sự biến đổi vật lí
cả hai sự biến đổi trên.
không phải sự biến đổi nào.
Đáp án : A
Dựa vào sự biến đổi vật lí và biến đổi hóa học.
Bánh mì nướng bị cháy là quá trình biến đổi hóa học vì chất trong bánh mì đã biến đổi thành than.
Đáp án A
Chọn khẳng định đúng trong các khẳng định sau?
Tổng khối lượng sản phẩm bằng tổng khối lượng các chất tham gia phản ứng.
Tổng khối lượng sản phẩm nhỏ hơn tổng khối lượng các chất tham gia phản ứng.
Tổng khối lượng sản phẩm lớn hơn tổng khối lượng các chất tham gia phản ứng.
Tổng khối lượng sản phẩm nhỏ hơn hoặc bằng tổng khối lượng các chất tham gia phản ứng.
Đáp án : A
Dựa vào định luật bảo toàn khối lượng.
Trong phản ứng hóa học, tổng khối lượng sản phẩm bằng tổng khối lượng các chất tham gia phản ứng.
Đáp án A
Tính khối lượng FeS tạo thành trong phản ứng của Fe và S, biết khối lượng của Fe và S đã tham gia phản ứng lần lượt là 8 gam và 3 gam.
11gam
10 gam
20 gam
5 gam
Đáp án : A
Dựa vào định luật bảo toàn khối lượng.
Ta có: m Fe + m S = m FeS
m FeS = 8 + 3 = 11g
Đáp án A
Điền vào chỗ trống: .......Al + .......O2 → .......Al2O3
2, 3, 1.
4, 3, 2.
4, 2, 3.
2, 3, 2.
Đáp án : B
Dựa vào cách cân bằng hóa học
4Al + 3O2 →→2Al2O3.
Đáp án B
Nung 1 kg đá vôi chứa 80% CaCO3, thu được 123,95 lít khí CO2 (đkc). Hiệu suất phân hủy CaCO3 là
80%
62,5%
50%
75%
Đáp án : B
Dựa vào số mol khí CO2 và phản ứng phân hủy CaCO3.
n CO2 = 123,95 : 24,79 = 5 mol
Khối lượng CaCO3 có trong 1 kg đá vôi là: 1.80% = 0,8kg = 800g
CaCO3 →CaO + CO2
5 ← 5 mol
H% = mCaCO3(TT)mCaCO3(LT).100=5.100800.100=62,5%
Đáp án B
Tỉ khối của chất X đối với không khí nhỏ hơn 1. X là khí nào sau đây?
O2
SO2
CO2
H2
Đáp án : A
Dựa vào công thức tính tỉ khối: dX/KK=MXMKK=MX29
Vì tỉ khối của chất X đối với không khí nhỏ hơn 1 nên MX nhỏ hơn MKK
Vậy khí X là H2.
Đáp án A
Mol là lượng chất có chứa bao nhiêu hạt vi mô (nguyên tử, phân tử, ...) của chất đó.
6,022×1022
6,022×1023
6,022×1024
6,022×1025
Đáp án : B
Dựa vào khái niệm mol.
Mol là lượng chất có chứa 6,022×1023 hạt vi mô của chất đó.
Đáp án B
Khối lượng mol của một chất là
khối lượng tính bằng gam của N nguyên tử hoặc phân tử chất đó.
khối lượng tính bằng kilogam của N nguyên tử hoặc phân tử chất đó.
khối lượng tính bằng gam của 1 nguyên tử hoặc phân tử chất đó.
khối lượng tính bằng kilogam của 1 nguyên tử hoặc phân tử chất đó.
Đáp án : A
Dựa vào khái niệm mol.
Khối lượng mol của một chất là khối lượng tính bằng gam của N nguyên tử hoặc phân tử chất đó.
Đáp án A
Khối lượng của 0,5 mol khí Cl2 là
71g
35,5g
70g
17,75g
Đáp án : B
Dựa vào công thức tính khối lượng: m = n.M
Khối lượng của 0,5 mol khí Cl2 = 0,5.71 = 35,5g
Đáp án B
Dung dịch là:
hỗn hợp gồm dung môi và chất tan.
hợp chất gồm dung môi và chất tan.
hỗn hợp đồng nhất gồm nước và chất tan.
hỗn hợp đồng nhất gồm dung môi và chất tan.
Đáp án : D
Dựa vào khái niệm dung dịch.
Dung dịch là hỗn hợp đồng nhất gồm dung môi và chất tan.
Đáp án D
Số mol trong 400ml NaOH 0,5M là
0,4M
0,2M
0,6M
0,8M
Đáp án : B
Dựa vào công thức nồng độ mol: CM = nV
Số mol NaOH = 0,4.0,5 = 0,2M
Đáp án B
Độ tan của muối NaCl ở 100oC là 40g. Ở nhiệt độ này dung dịch bão hòa NaCl có nồng độ phần trăm là
28%
26,72%
28,5%
20,05%
Đáp án : C
Dựa vào công thức tính độ tan
Nồng độ phần trăm NaCl là = mctanmdd.100=4040+100.100=28,5%
Đáp án C
Để xác định được mức độ phản ứng nhanh hay chậm người ta sử dụng khái niệm nào sau đây?
Tốc độ phản ứng.
Cân bằng hoá học.
Phản ứng một chiều.
Phản ứng thuận nghịch.
Đáp án : A
Dựa vào khái niệm tốc độ phản ứng.
Để xác định được mức độ phản ứng nhanh hay chậm người ta sử dụng khái niệm tốc độ phản ứng.
Đáp án A
Chất làm tăng tốc độ phản ứng hoá học mà không bị biến đổi chất được gọi là
Chất xúc tác.
Chất sản phẩm.
Chất tham gia.
Chất ức chế.
Đáp án : A
Dựa vào các yếu tố làm tăng tốc độ phản ứng.
Chất làm tăng tốc độ phản ứng hóa học mà không bị biến đổi chất là chất xúc tác.
Đáp án A
Tính khối lượng nước tạo thành khi đốt cháy hết 65 gam khí hydrogen theo sơ đồ phản ứng sau
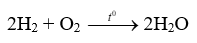
Tính số mol khí hydrogen và dựa vào phản ứng để tính khối lượng nước tạo thành.
n H2 = 652=32,5mol
Theo phản ứng: n H2 = n H2O = 32,5 mol
m H2O = 32,5.18 = 585g
Cho 8,45g Zn tác dụng với 5,95 lít khí Cl2 (đkc). Hỏi chất nào sau phản ứng còn dư? Giải thích?
Tính số mol khí Cl2 và Zn và dựa vào phản ứng để xác định chất hết, chất dư.
n Cl2 = 5,9524,79=0,24mol; n Zn = 8,4565=0,13mol
Zn + Cl2 → ZnCl2
0,13 0,24
Ta thấy: n Cl2 > n Zn => Cl2 dư; Zn hết
Từ muối NaCl, nước cất và những dụng cụ cần thiết, hãy nêu cách pha chế 150 gam NaCl có nồng độ 30%.
Dựa vào cách pha chế dung dịch.
Khối lượng NaCl có trong dung dịch là: 150.30% = 45g
Cách pha:
- Lấy 45g chất rắn NaCl.
- Hòa tan 45g NaCl rắn vào 105ml nước cất. Khuấy đều thu được dung dịch thu được 150 gam dung dịch NaCl 30%.
Cho 50 ml dung dịch AgNO3 vào 100 g dung dịch 1,9% muối chloride của một kim loại M hóa trị II, phản ứng vừa đủ thu được 5,74 g kết tủa AgCl. Biết PTHH của phản ứng là:
MCl2+2AgNO3→M(NO3)2+2AgCl↓
a) Xác định kim loại M.
b) Xác định nồng độ mol dung dịch AgNO3.
a) Gọi số mol muối MCl2 là a.
Khối lượng muối: 100.1,9%100%=1,9(g).
MCl2+2AgNO3→M(NO3)2+2AgClTheoPTHH:1212(mol)Phanung:a→2a→a→2a(mol)Taco:a=5,742.143,5=0,02(mol)(1)(M+2.35,5).0,01=0,95=>M=24
Vậy kim loại cần tìm là Mg.
b) Nồng độ của dung dịch AgNO3: 2.0,020,05=0,8(M).
Mẹo tìm đáp án nhanh
Search Google: "từ khóa + baitap365" Ví dụ: "Bài 5 trang 13 SGK Vật lí 12 baitap365